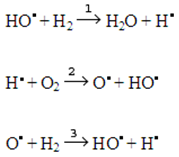|
01.01.15
Конкурс РФФИ 2015 года
Российский фонд фундаментальных исследований (РФФИ) проводит конкурс проектов участия российских ученых в научных мероприятиях, проводимых за рубежом 2012 года. Заявки принимаются до 01.11.2015 Внимание Вышла в продажу вторая редакция книги "Twenty-First Century. General Chemistry" |
Home / Доклады и выступления / Доклад Доклад22 августа 2010 г В наших предыдущих докладах на заседаниях Американского Химического общества и их обобщениях в книгах изданных в 1990 - 2007 мы подробно описали результаты наших работ. В ходе этих работ нам удалось понять как образуется химическая связь, как протекает химическая реакция и понять механизм катализа. Конечным результатом этих работ на сегодня (2010г.) является то, что нам удалось понять физический смысл основных правил и законов, открытых в ходе изучения основных химических явлений (правил Льюиса, правил Резонанса, правил валентности, правил Семенова - Поляни, Периодического закона и т.д.) и предложить доступное для учащихся школ объяснение этого физического смысла. Физический смысл правил Льюиса.Правила Льюиса, гласящие, что атомы стремятся достроить свои оболочки до оболочек инертных газов, имеют антропофизический смысл. В ходе экспериментальны исследований, предшествующих нашим, было доказано, что электроны, окружающие ядра атомов, располагаются слоями и было определено количество электронов в каждом из слоев. При анализе этих данных в рамках периодического закона следовало, что при движении вдоль периода увеличивается на единицу протона заряд ядра и увеличивается на единицу количество электронов во внешнем электронном слое. Эта закономерность имела границы в зависимости от номера периода. Для первого периода эта закономерность наблюдалась только для двух элементов ( ) для второго и третьего периода для 8-ми элементов, для 4-го и 5-го периода 18элементов. В ходе изучения природы химической связи нами было доказано, что при образовании ковалентной химической связи внешний электрон одного атома входит во внешнюю оболочку другого атома. Т.е. образование химической связи между атомами возможно только в том случае, если внешние оболочки этих атомов являются незаполненными, т.е. количество электронов в них меньше максимально возможного. Максимально возможное количество электронов во внешнем слое содержится у инертных газов. Образование химических связей одного атома с другими атомами прекращается, когда количество электронов во внешней оболочке этого атома становиться равным количеству электронов ближайшего к нему инертному газу. Физический смысл правил валентности.В рамках принятых квантово - химических объяснений утверждалось, что валентность элементов определяется количеством в верхнем электронном слое электронов с противоположными спинами. Физический смысл спина электрона был не известен. После выяснения физического смысла правил Льюиса стал понятен физический смысл правил валентности. Валентность определяется с одной стороны количеством электронов во внешнем слое элемента и с другой стороны количеством электронов, которое может принять данный атом в уже существующие электронные оболочки с выигрышем энергии. Физический смысл правил резонанса.Правила резонанса использовались для объяснения строения соединений, которые могут быть описаны в рамках правил Льюиса, не одной, а несколькими структурными формулами. Согласно правилам резонанса реальная структура данного вещества является суперпозицией всех возможных в рамках правил Льюиса структур. Понятие суперпозиция физического смысла не имело. В рамках правил резонанса изомеризация между структурами исключалась. На основании обобщения материала опубликованного в литературе по электронной изомеризации нами было показано, что все явления, описываемые правилами резонанса, объясняются электронной изомеризацией. Физический смысл правил Семенова - Поляни.Правило Семенова - Поляни заключается в утверждении, что чем больше тепловой эффект химической реакции, тем выше ее скорость в однотипных реакциях. В рамках теории переходного состояния, предшествующей разработанной нами теории элементарных взаимодействий, физический смысл этого правила был непонятен. В рамках теории элементарных взаимодействий было показано, что химические реакции протекают по цепному механизму, активными частицами в котором являются атомы с незаполненными электронами внешними оболочками. В качестве примера рассмотрим взаимодействие водорода с кислородом. Если при комнатной температуре поместить в закрытый сосуд кислород и водород, то взаимодействие между этими двумя газами не произойдет. Однако если подействовать на эту смесь электрическим зарядом, или возбудить ее каким-либо другим способом, произойдет взрыв. Эта реакция протекает по цепному механизму через стадии зарождения, развития и обрыва цепи. Зарождение цепи - это процесс начального образования радикалов под действием внешнего возмущения или наличия третьих частиц (например, пылинок или металлов, Me): Н2 + О2 → 2НО• Н2 + Me → 2Н• + Me О2 + О2 → О• + О3 где Мe - металл Развитие цепи может быть простым (когда взаимодействие радикала с молекулой порождает снова один радикал) или разветвленным (когда такое взаимодействие приводит к появлению более одного радикала).
На стадиях 2 и 3 при взаимодействии радикала с молекулой образуются два новых радикала, и происходит процесс разветвления цепи. Вследствие выделения тепла газовая смесь быстро разогревается, что приводит к экспоненциальному ускорению реакции, которое в свою очередь, обуславливает еще большее тепловыделение и соответствующее увеличение температуры реакционной смеси. Резкое и быстрое (мгновенное) возрастание температуры приводит к такому же быстрому и резкому увеличению давления в системе, что и вызывает взрыв. Согласно общей схеме химических превращений, энергия, выделяющаяся на предыдущих стадиях реакции, может расходываться на разрушение химических связей. В таком случае помимо ранее рассмотренного пути превращения можно предположить и другой путь, например, для взаимодействия дейтерия и молекулярного водорода:
Здесь символом * обозначена термически активированная молекула. Стадия 4, на которой происходит разрушение слабой химической связи в комплексе [DHH] протекает с поглощением энергии, выделившейся при образовании новых химических связей на предыдущих стадиях. Влияние давления на скорость реакции доказывает существование такого пути превращения. При увеличении давления возрастает скорость диссипации энергии за счет роста числа молекул в единице реакционного объема, т.е. роста концентрации, а это в свою очередь уменьшает долю активных частиц в смеси. Реакции, в которых выделившаяся на экзотермических стадиях энергия далее расходуется на последующих эндотермических маршрутах, могут быть названы химически активированными реакциями. Большая часть радикальных реакций с ненасыщенными молекулами (имеющими двойные и тройные связи) как раз и относятся к такого рода превращениям. Основной особенностью этих реакций является независимость их скорости от температуры, поскольку энергия активации этих реакций, как правило, равна нулю. Количество электронных изомеров с ослабленной исходной химической связью определяется разностью в энергиях связи исходной и образуемой в ходе реакции. Чем больше энергия образующейся в ходе реакции новой связи, тем больше концентрация этого изомера в равновесной смеси согласно термодинамике. Физический смысл и роль катализатора в химических реакциях.Согласно механизму химической реакции скорость реакции определяется концентрацией промежуточного соединения и активных частиц. Условно катализаторы можно разбить на две группы. К первой группе относятся вещества, которые в условиях реакции дают значительно больше активных частиц ведущих цепной процесс. Наглядные примеры щелочной и кислотный гидролиз сложных эфиров. Ко второй группе относятся катализаторы, увеличивающие концентрацию промежуточного соединения. Эти катализаторы образуют комплекс с обеими исходными насыщенными молекулами и электронная изомеризация протекает через промежуточное образование химических связей с катализатором. Кроме того роль химической активации также возрастает с выигрышем энергии в ходе реакции, что позволяет понять физический смысл правил Семенова - Поляни. Физический смысл Периодического ЗаконаСогласно формулировке Менделеева свойства элементов меняются периодически при росте их атомного веса. После работ Мозли этот закон переформулировался: свойства элементов меняются периодически при росте их зарядов ядер. Периодический Закон являлся великим открытием, систематизировавшим, не только элементы, но и простые и сложные вещества, полученные из этих элементов. Более того он позволил Менделееву предсказать физические свойства еще не открытых элементов. После открытия Резерфордом строения атома Периодический Закон стал пародоксальным законом по уровню пародоксальности равным Закону эквивалентности инерционной и гравитационной масс открытых Ньютоном. Физический смысл -это причинно - следственные связи между явлениями. Парадоксальность этих законов заключалось в том, что представлялось невозможным даже предположить в виде безумной гипотезы какую- либо причинно - следственную связь для объяснения периодической зависимости физических и химических свойств элементов и веществ из них образуемых от зарядов их ядер окруженных роем электронов. После выяснения физического смысла правил Семенова - Поляни нам стало понятно, что химические свойства веществ их реакционная способность определяются разницей в энергии связи образуемой и разрываемой в ходе реакции. Экспериментальные данные и расчеты по модели совпадающие качественно с экспериментальными данными показали, что энергия химической связи определяется первыми потенциалами ионизации атомов. Экспериментальные данные по первым потенциалам ионизации атомов элементов при росте зарядов ядер менялись периодически с ростом зарядов ядер. Т.е. в результате решения вопроса как образуется химическая связь и как протекает химическая реакция нам удалось понять и объяснить физический смысл Периодического Закона. |